Bottom Line
O tratamento do adenocarcinoma de esôfago vem experimentando considerável avanço nos últimos anos, tanto do ponto de vista de terapia multimodal, quanto em técnicas e táticas cirúrgicas. Embora ainda com resultados desanimadores nos pacientes com diagnóstico de doença avançada, nos casos de tumores localizados ou localmente avançados, há a expectativa de cada vez mais se atingir a cura.

Héber Salvador de Castro Ribeiro é Titular do Departamento de Cirurgia Abdominal do AC Camargo Cancer Center
Por Héber Salvador de Castro Ribeiro, Igor Correia de Farias, Wilson Luiz da Costa Jr, Alessando Landskron Diniz, André Luis de Godoy, Silvio Melo Torres e Felipe José Fernández Coimbra
1 - Titular do Departamento de Cirurgia Abdominal do AC Camargo Cancer Center – São Paulo/SP
2 - Diretor do Departamento de Cirurgia Abdominal do AC Camargo Cancer Center – São Paulo/SP
Resumo
O câncer de esôfago é a oitava neoplasia mais incidente no mundo e a sexta causa de óbito por câncer. Um de seus tipos histológicos, o adenocarcinoma de esôfago tem registrado incidência crescente, especialmente em países desenvolvidos.
Neste artigo, os autores discorrem sobre a epidemiologia e fatores de risco do adenocarcinoma esofágico, discutem seu diagnóstico e estadiamento, além de traçar um panorama dos progressos terapêuticos e principais avanços cirúrgicos.
Afinal, o que mudou com o tratamento multimodal e as novas táticas cirúrgicas?
Na cirurgia, o maior avanço veio com a técnica minimamente invasiva introduzida por Cuschieri em 1992. Desde então, sucessivas publicações têm demonstrado não só a equivalência em termos de segurança oncológica, mas também a redução significativa da morbidade cirúrgica da esofagectomia quando um tempo ou todo o procedimento é feito de maneira minimamente invasiva.
Em relação às estratégias terapêuticas, crescem evidências que apontam o benefício do tratamento multimodal para pacientes com lesões localmente avançadas, com extensão do tumor primário além da camada muscular (T2) ou comprometimento linfonodal regional. Os dados disponíveis sugerem ganho significativo de sobrevida global, aumento de ressecções R0 e de resposta patológica completa.
Em conclusão, o tratamento do adenocarcinoma de esôfago vem experimentando considerável avanço nos últimos anos, tanto do ponto de vista de terapia multimodal, quanto em técnicas e táticas cirúrgicas. Embora ainda com resultados desanimadores nos pacientes com diagnóstico de doença avançada, nos casos de tumores localizados ou localmente avançados, há a expectativa de cada vez mais se atingir a cura.
Palavras-chave: ‘adenocarcinoma esofágico’, ‘fatores de risco’, diagnóstico, ‘tratamento multimodal’, ‘táticas cirúrgicas’,
Epidemiologia e fatores de risco
O câncer de esôfago é a oitava neoplasia mais incidente no mundo e a sexta causa de óbito por câncer1. Um dos seus tipos histológicos, o adenocarcinoma, tema desta discussão, tem registrado aumento progressivo de sua incidência, especialmente em países desenvolvidos2,3.
Parcela cada vez maior da população mundial é exposta aos fatores de risco para o adenocarcinoma de esôfago, como Doença do Refluxo Gastroesofágico (DRGE) sintomática, obesidade, Esôfago de Barrett, tabagismo e uma dieta pobre em frutas e vegetais4. Quanto à DRGE, a sua relação com a neoplasia é bem estabelecida, porém até 40% desses pacientes podem ser assintomáticos. Provavelmente, há uma superposição de fatores entre este diagnóstico e a obesidade, com um aumento do risco com essa associação5.
O Esôfago de Barrett representa um diagnóstico endoscópico e anatomopatológico. É necessária a caracterização de epitélio cor de “salmão” em localização cefálica em relação à junção esôfago-gástrica e o achado de epitélio colunar tipo intestinal substituindo o epitélio estratificado pavimentoso esofágico, em exame anatomopatológico. Essas alterações estão relacionadas ao desenvolvimento do adenocarcinoma, com risco estimado de cerca de 0,5% ao ano6. Este risco está aumentado quando há achado associado de displasia de alto grau, cuja progressão para adenocarcinoma ocorre em cerca de 40% dos casos7.
Diagnóstico e Classificação
O adenocarcinoma de esôfago se apresenta tardiamente, na maioria dos casos. Isso ocorre pelo atraso no diagnóstico e pela propensão da neoplasia em se disseminar à distância mesmo em fases mais iniciais8. Os pacientes normalmente relatam sintomas de DRGE e evolução recente com disfagia, muitas vezes não relacionada à perda significativa de peso.
As ferramentas de estadiamento incluem TC de tórax, abdome, pelve e, em alguns casos, cervical, broncoscopia, eco-endoscopia e PET-CT. Em nossa rotina, empregamos tomografias de tórax, abdome e pelve para todos os casos. A imagem cervical é obtida em lesões torácicas altas e cervicais ou em tumores mais baixos com indícios clínicos de linfonodomegalia em região cervical. Indicamos a broncoscopia em lesões torácicas altas e médias, para afastar a possibilidade de invasão da árvore brônquica. A ecoendoscopia fica reservada para situações em que não se identifica espessamento da parede esofágica nas tomografias realizadas, fazendo-se necessário melhor avaliação do estadiamento T e N, com melhor definição da abordagem terapêutica9. O PET-CT tem sido costumeiramente empregado nos casos de tumores localmente avançados, especialmente os elegíveis para tratamento multimodal. Este exame parece modificar a conduta terapêutica em até 25% dos pacientes, demonstrando metástases à distância insuspeitas nos demais exames, bem como determinando melhor as rotas de disseminação linfonodal em alguns casos.
A classificação anatômica de Siewert (1987), embora difícil de ser aplicada em determinadas situações, especialmente no cenário pré-operatório, é ainda a mais utilizada. Os tumores Siewert I são considerados os verdadeiros tumores do esôfago distal e os tipos II (cárdia) e III (fundo gástrico) são tratados mais frequentemente como tumores gástrico, sendo submetidos à gastrectomia total e esofagectomia distal em boa parte dos casos, mantendo ainda sim a radicalidade oncológica.
Tratamento multimodal
O prognóstico de um paciente com adenocarcinoma esofágico depende essencialmente do estadiamento da neoplasia ao diagnóstico2. As casuísticas de tratamento cirúrgico exclusivo estão associadas a taxas de sobrevida global que não ultrapassam 35% em 5 anos, com recidiva predominantemente à distância, porém também com altas taxas de recidiva locorregional10. Pacientes com lesões localmente avançadas, definidas como aquelas em que a extensão do tumor primário vai além da camada muscular – T2, ou em que há comprometimento linfonodal regional, são candidatos às modalidades de tratamento multimodal11.
Existem diversos estudos prospectivos e randomizados que investigaram a associação de quimioterapia peri-operatória (neoadjuvante e adjuvante) intercalada com o tratamento cirúrgico; outros descrevendo a associação de quimioterapia e radioterapia neoadjuvantes seguidos de cirurgia e, ainda, alguns estudos investigando o papel da adjuvância após tratamento cirúrgico inicial, neste caso com evidência extremamente limitada.
Tratamento neoadjuvante pode ser definido como a adoção de quimioterapia ou a associação de quimioterapia e radioterapia previamente a um tratamento cirúrgico com intuito curativo de um tumor ressecável não metastático. Ele está associado a alguns benefícios bem estabelecidos, como aumento de ressecções curativas R0, downstaging linfonodal e do tumor primário, maior aderência ao esquema terapêutico, tratamento precoce da doença micrometastática e avaliação da resposta ao tratamento quimioterápico in vivo, avaliando de um modo geral a biologia tumoral e o prognóstico da doença, evitando procedimentos cirúrgicos mórbidos e desnecessários.
Quimioterapia peri-operatória
Existem pelo menos quatro grandes estudos prospectivos e randomizados que incluíram um número significativo de pacientes com adenocarcinoma de esôfago cujos resultados devem ser comentados em mais detalhes. O primeiro deles foi o estudo americano INT 113, que inscreveu 467 pacientes entre 1990 e 1995 e investigou o papel da quimioterapia (QT) neoadjuvante com 3 ciclos de cisplatina e 5-Fluoracil. Neste estudo, metade dos indivíduos tinham diagnóstico de adenocarcinoma. Não houve diferença estatística de sobrevida mediana ou em 3 anos entre os grupos. Apenas um aumento de ressecções R0 foi observado com a adição de quimioterapia entre os indivíduos que chegaram a ser operados. Algumas críticas relacionadas a este estudo incluem o atraso no tratamento cirúrgico após a quimioterapia, um número maior de tumores nos estádios I e II e o fato de cerca de metade dos pacientes ter recebido pelo menos um ciclo de QT no pós-operatório12.
Outro estudo foi o MRC (UK Medical Research Council) OE02 “trial”, com 802 indivíduos entre 1992 e 1998. A comparação foi entre tratamento cirúrgico exclusivo e a neoadjuvância com 2 ciclos de cisplatina e 5-Fluoracil. Cerca de dois terços dos pacientes tiveram diagnóstico de adenocarcinoma. Aqueles tratados com esquema multimodal tiveram sobrevida mediana de 16,8 meses versus 13,3 meses do grupo com cirurgia apenas, com redução do risco de óbito de 16% (HR 0,84; p=0,03). Da mesma maneira que no estudo anterior, críticas importantes devem ser mencionadas, como o resultado numérico de sobrevida dos grupos e o fato de cerca de 10% dos pacientes ter recebido também tratamento com radioterapia13.
Dois estudos randomizados recentes investigaram o papel da quimioterapia neoadjuvante e adjuvante em pacientes com adenocarcinoma de esôfago distal e gástrico. O primeiro deles, o MAGIC Trial, contou com 503 indivíduos e o esquema de quimioterapia proposto foi de ECF (Epirrubicina, Cisplatina e 5-Fluoracil), três ciclos antes e três após a cirurgia. Houve ganho de sobrevida global em 5 anos de 13% para o braço de pacientes do tratamento multimodal (36% vs. 23%). No entanto, apenas 25% deles tiveram tumores de esôfago distal ou transição esofagogástrica e neste subgrupo o ganho de sobrevida não foi significativo14. Houve ainda um estudo francês, o FFCD Trial, com 169 pacientes, novamente demonstrando 14% de ganho de sobrevida com quimioterapia pré e pós-operatória, porém com duas drogas (Cisplatina e 5-Fluoracil). Importante ressaltar que os dados deste estudo são aplicáveis para os pacientes com adenocarcinoma de esôfago distal e TEG, visto que 75% da população do estudo apresentavam lesões nestas localizações e a análise de subgrupos demonstrou ganho de sobrevida para estes indivíduos15.
Um estudo mais recente e muito importante, apresentado na ASCO 2017 e publicado na Lancet Oncology 2019, o FLOT4 avaliou 716 pacientes randomizados em dois braços, o primeiro realizou FLOT (5-FU + Leucovorin + Oxaliplatina + Docetaxel) peri-operatório, sendo 4 ciclos pré e 4 ciclos pós e o segundo braço submetido a ECF/ECX (Epirrubicina + Cisplatina + 5-FU ou Xeloda) peri-operatório, sendo 3 ciclos pré e 3 ciclos pós. Importante dados deste estudo é que sua população era composta em mais de 50% dos casos em ambos os braços de tumores de TEG. Os dados foram bastante favoráveis e robustos em favor do esquema FLOT, com ganho de sobrevida global mediana em torno de 15 meses (50 versus 35) e ganho de sobrevida global de 9% (45 versus 36), com HR para sobrevida global de 0,7735.
Quimioterapia e Radioterapia neoadjuvantes
Existem também três estudos randomizados principais que investigaram o papel da radioterapia associada à quimioterapia neoadjuvantes, seguidas de cirurgia. O primeiro foi publicado em 2005 e envolveu 256 pacientes, 62% com adenocarcinomas. Não houve ganho significativo de sobrevida global mediana (22 meses versus 19 meses). Observou-se aumento significativo de ressecções R0 e de tumores N0 (downstaging linfonodal) com o tratamento multimodal. O caráter multicêntrico do estudo e a dose de radioterapia administrada, de 35 Gy, e, provavelmente, a justificativa da baixa taxa de resposta patológica completa são algumas das justificativas para o resultado negativo. Ainda assim, um ganho significativo de sobrevida global foi primeiramente observado para os carcinomas epidermoides (CEC)16.
O primeiro estudo a demonstrar ganho expressivo de sobrevida com o tratamento multimodal foi o americano CALGB 9781, publicado em 2008. Com uma amostra estimada de 475 pacientes, o estudo foi interrompido com apenas 56 pacientes por dificuldade de recrutamento. Predominaram os casos de adenocarcinoma e a dose proposta de radioterapia foi de 50,4Gy, em 28 sessões de 180cGy. A sobrevida mediana do grupo de tratamento multimodal foi de 4,5 anos (1,8 anos no de cirurgia exclusiva) e a sobrevida global em 5 anos foi de 39% (16% para os cirúrgicos exclusivos). Observaram-se maior taxa de resposta patológica completa (33%), de ressecções R0 e tumores N017.
O Cross Trial, publicado em 2012, é o estudo randomizado mais recente a investigar o papel de quimioterapia e radioterapia concomitantes no cenário neo-adjuvante, e também o de resultados mais consistentes. A quimioterapia consistiu num esquema moderno de bom perfil de toxicidade (Carboplatina e Paclitaxel) e a dose de radioterapia foi de 41,4Gy, divididas em 23 sessões de 180cGy. Dentre os 364 pacientes, 75% tinham adenocarcinoma. Houve ganho significativo de sobrevida global (47% vs 34%), além de um aumento de 23% de ressecções R0, de 44% de tumores N0 e ainda 29% de casos com resposta patológica completa. Para os subgrupos dos adenocarcinomas, essa taxa de reposta patológica completa foi de 23%. As taxas de morbimortalidade foram semelhantes e o braço de pacientes tratados com cirurgia exclusiva apresentou sobrevida superior à observada em todas as outras séries, com seguimento mediano de aproximadamente 4 anos18.
Estudos comparativos
Dois estudos compararam as duas modalidades de tratamento multimodal, de quimioterapia pré-operatória seguida de cirurgia versus quimioterapia e radioterapia seguidas de cirurgia. No entanto, ambos os estudos, um alemão com 119 pacientes e um australiano com 72 pacientes, não apresentaram poder estatístico adequado para as análises pretendidas. As diferenças de sobrevida não foram significativas entre os grupos. No estudo alemão, ela foi um pouco melhor entre os pacientes que fizeram radioterapia, porém o dado não foi significativo, além deste mesmo grupo ter ainda apresentado maior mortalidade pós-operatória. A adição de radioterapia se associou em ambos os estudos a mais ressecções R0 e a um significativo clareamento linfonodal19,20.
Em meta-análise atualizada em 2011 demonstrou-se redução de risco de óbito pela neoplasia com a realização de quimioterapia neoadjuvante de 13%, um ganho absoluto de sobrevida de 5,1% em 2 anos. Quando o tratamento neoadjuvante foi de radioterapia associada à quimioterapia, a redução de risco foi de 22%21. Portanto, fica a pergunta de qual seria, então, a melhor estratégia de tratamento multimodal para os tumores de esôfago distal/TEG, RXT/QT baseados nos esquema CROSS Trial ou QT peri-operatória baseadas no esquema FLOT4 Trial. Ainda não temos esta resposta atualmente, apesar de existir um tendência em favor do esquema de QT peri-operatória (FLOT) nos principais centros de tratamento de câncer do nosso meio e esta é a conduta preferencial do nosso serviço. Porém, dentro de mais alguns anos teremos uma resposta a esta pergunta, que será trazida pelo ESOPEC Trial (NCT02509286) que está randomizando pacientes para esta comparação, FLOT versus CROSS.
Tratamento adjuvante
A evidência para tratamento adjuvante após ressecção de adenocarcinoma de esôfago distal ou de transição esofagogástrica é bastante pobre22. O único estudo que leva a alguma recomendação é o INT0116 (MacDonald Trial), que investigou o papel de quimioterapia e radioterapia adjuvantes após cirurgia para câncer gástrico ou de transição. No entanto, esta é uma interpretação controversa, visto que apenas 20% da amostra do estudo era de indivíduos com lesões em transição e a cirurgia realizada em todos foi uma gastrectomia23.
Apesar da grande discussão sobre o papel da ressecção cirúrgica no câncer de esôfago, especialmente após resposta clínica completa em casos de carcinoma espinocelular, nossa posição ainda é a de indicar a esofagectomia a todos os pacientes clinicamente aptos ao tratamento cirúrgico, exceto aos que apresentam progressão sistêmica após neoadjuvância24. Não há dados de literatura que suportem o uso de radioterapia e quimioterapia exclusivas como tratamento curativo para o adenocarcinoma do esôfago e de transição, motivo desta revisão. Esta reposta, porém, nos será dada pelo SANO Trial36.
Historicamente, a esofagectomia é considerada procedimento complexo, com várias táticas e abordagens cirúrgicas descritas, apresentando altas taxas de morbimortalidade. O desenvolvimento e aprimoramento das técnicas anestésicas e de cuidados intensivos, bem como a padronização do procedimento operatório e, especialmente, a concentração destas cirurgias em centros de grande volume foram responsáveis pela progressiva redução destes números, atingindo percentuais de 30 – 40% de risco de complicações pós-operatórias e mortalidade abaixo de 5% nos dias atuais. Sem dúvida, este é o procedimento onde a frequência de execução por serviço e cirurgião mais impactam nos resultados pós-operatórios, com redução estimada da taxa de mortalidade de cerca de 5 vezes entre centros que realizam mais que 20 esofagectomias anuais25, 26.
Condicionamento peri-operatório
Os resultados e desfechos oncológicos estão diretamente relacionados a melhor avaliação de risco cirúrgico, bem como melhor seleção dos pacientes, somado a um melhor entendimento no pré-condicionamento cirúrgico destes pacientes. Suporte nutricional adequado, no pré e pós-operatória, bem como um preparo com condicionamento respiratório e muscular com a equipe de fisioterapia são fundamentais.
Estudo publicado em 2015 pelo grupo do professor Yuko Kitagawa demonstrou que a nutrição enteral precoce no pós-operatório esteve associada a menor incidência de complicações infecciosas pulmonares bem como a uma menor perda de peso quando comparada com a nutrição parenteral38. No Departamento de Cirurgia Abdominal do AC Camargo Cancer Center temos como rotina a realização de nutrição enteral precoce, seja por sonda naso-enteral passado logo após a confecção da anastomose cervical esôfago-gástrica (Técnica de McKeown) ou por jejunostomia realizada ao final da cirurgia, sendo nossa primeira opção sempre a sonda naso-entérica.
Táticas Cirúrgicas
Há grande discussão na literatura sobre qual modalidade de abordagem cirúrgica seria mais adequada para o adenocarcinoma esofágico, se a esofagectomia transtorácica (ETT) ou a trans-hiatal (ETH). Como a maioria destes tumores acontecem no terço distal, as cadeias linfonodais mais acometidas incluem as mediastinais inferiores, além das para-cárdicas e ao longo da pequena curvatura e artéria gástrica esquerda. A incidência de disseminação linfonodal acima da carina é relativamente baixa, embora haja grande discrepância entre estudos ocidentais e orientais. Obviamente, quanto mais proximais e invasivos os tumores são na parede esofágica, maior o risco de acometimento linfonodal mediastinal alto27.
Este tópico foi investigado por alguns estudos prospectivos e randomizados, o de maior peso publicado em 2002 por um grupo holandês28. Nele, 220 pacientes com adenocarcinoma de esôfago médio e distal foram randomizados para a ressecção via transtorácica ou trans-hiatal abertas. Este estudo foi bastante criticado principalmente pelo estadiamento considerado incompleto no pré-operatório (nem todos os pacientes realizavam tomografia computadorizada) e pela desproporção dos procedimentos, uma vez que os pacientes do grupo de esofagectomia trans-torácica receberam cirurgia estendida, incluindo ressecção enbloc do ducto torácico e veia ázigos. Na análise por intenção de tratamento, não houve diferença estatisticamente significativa em sobrevida. Além disso, a morbidade foi maior no grupo de ETT, mas a mortalidade intra-hospitalar foi semelhante. Em 2007 foi publicada atualização deste estudo, com análise de sobrevida estratificada por acometimento linfonodal e sítio primário, de acordo com a classificação de Siewert29. Na análise geral, o ganho numérico de sobrevida do grupo pós ETT continuou sem diferença estatística, mesmo em tumores Siewert I (51% x 37%, p=0,33). O mesmo foi observado para pacientes sem acometimento linfonodal (N0), assim como para aqueles com mais de 8 linfonodos positivos na peça cirúrgica. No entanto, para o subgrupo de pacientes que apresentavam entre 1 e 8 linfonodos comprometidos, a diferença de sobrevida de 64% para 23% a favor do grupo de ETT foi estatisticamente significativa, de onde concluíram que a abordagem mais agressiva beneficiaria justamente os pacientes neste cenário, apesar da dificuldade de se realizar esta estratificação no pré-operatório. Estes achados não se reproduziram em meta-análise posteriormente publicada, permanecendo este debate em aberto30.
Estes dados foram produzidos, no entanto, sem levar em consideração o maior avanço técnico neste campo, que foi a cirurgia minimamente invasiva introduzida por Cuschieri em 199231. Desde então, sucessivas publicações têm demonstrado não só a equivalência oncológica, mas também uma redução significativa da morbidade cirúrgica (incluindo tempo de internação em UTI e hospitalar) da esofagectomia quando um tempo ou todo o procedimento é feito por esta via.
A evidência mais robusta até o momento reside em estudo prospectivo e randomizado publicado em 2012, no qual pacientes com câncer de esôfago médio e distal (incluindo CEC e adenocarcinoma) foram aleatorizados para ETT aberta ou minimante invasiva (toracoscopia/laparoscopia)32. Embora com um número pequeno de pacientes recrutados, demonstrou-se que o grupo de cirurgia toracoscópica apresentou significativamente menos infecções pulmonares pós-operatórias, menor tempo de internação e melhor qualidade de vida, sem, no entanto, reduzir a mortalidade ou impactar a sobrevida a longo prazo.
Este estudo e outras publicações vêm demonstrando os benefícios da realização da cirurgia em posição prona, incluindo o melhor campo operatório, com mais ergonomia ao cirurgião, permitindo menos punções e, principalmente, não sendo necessário a ventilação seletiva. Teoricamente, este posicionamento permitirá inclusive um encurtamento da curva de aprendizado do procedimento. Sua principal desvantagem reside na dificuldade técnica de acesso ao mediastino em caso de necessidade de conversão de emergência33.
Mais recentemente, a cirurgia robótica vem ganhando espaço como ferramenta de importante valor para a realização da esofagectomia minimamente invasiva. A princípio, seu grande diferencial é a visão tridimensional que o console permite ao cirurgião, com maior precisão dos movimentos e segurança na dissecção, além do conforto durante o ato operatório. O prolongado tempo cirúrgico, associado ao custo ainda desproporcional quando comparado à toracoscopia/laparoscopia convencional, retardam a difusão mais ampla desta opção terapêutica34. Um trabalho publicado em 2012 na Trials, o ROBOT Trial, comparando exatamente a via de acesso robótica transtorácica e laparoscópica abdominal (RAMIE) versus a via aberta convencional em ambos os campos operatórios (OPEN), demonstrou menor taxa de complicações pós-operatórias, principalmente cardio-pulmonares, menor perda de sangue no intra-operatório, menor dor pós-operatória, bem como recuperação da qualidade de vida e da funcionalidade mais precoce em favor da via robótica, no entanto, sem diferença em termos de desfechos oncológicos37. Uma crítica feita a este estudo seria a comparação da via minimamente invasiva por cirurgia robótica com a via aberta convencional em ambos os campos operatórios, torácico e abdominal. Talvez a melhor comparação seria a via robótica com a via laparoscópica. Vale lembrar que tanto a cirurgia robótica quanto a cirurgia laparoscópica e aberta convencional são ferramentas importantes que não competem, mas pelo contrário, se somam ao grande armamentário que possuímos hoje no tratamento desta doença, cada uma tem sua indicação mais adequada, sendo esta realizada caso a caso.
Conclusão
O tratamento do adenocarcinoma de esôfago vem experimentando considerável avanço nos últimos anos, tanto do ponto de vista de terapia multimodal, quanto em técnicas e táticas cirúrgicas. Embora ainda com resultados desanimadores nos pacientes com diagnóstico de doença avançada, nos casos de tumores localizados ou localmente avançados, há a expectativa de cada vez mais se atingir a cura. Os desafios que se impõem diariamente aos profissionais ligados a este cuidado são, como em outras áreas, a seleção de cada caso para a sequência terapêutica ideal e, em nosso meio, a garantia do acesso igualitário de todos aos progressos terapêuticos.
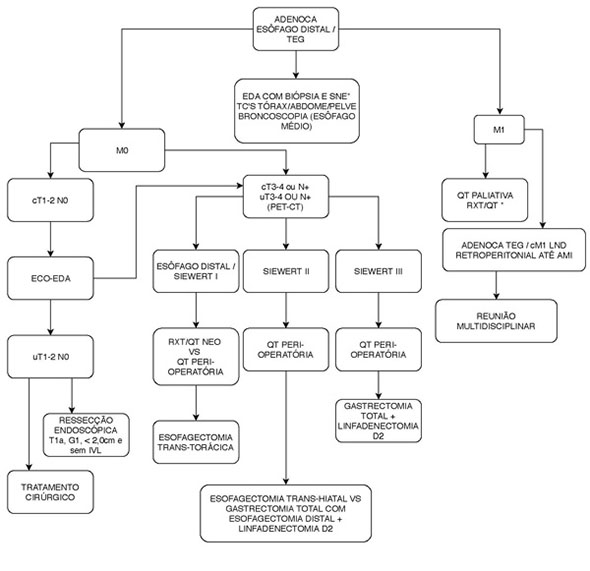
Figura 1. Fluxograma de tratamento multimodal do Adenocarcinoma de esôfago e TEG do Departamento de Cirurgia Abdominal do A.C. Camargo Câncer Center9.
Os autores declaram não haver conflitos de interesse nesta publicação.
Referências:
1 – Ferlay J, Shin HR, Bray F, Forman D, Mathers C, Parkin DM. Estimates of worldwide burden of cancer in 2008. GLOBOCAN 2008. Int J Cancer 2010; 127: 2893-917.
2 – Jemal A, Siegel R, Ward E, Hao Y, Xu J, Thun MJ. Cancer statistics 2009. CA CancerJ Clin 2009; 59: 225-49.
3 – Lepage C, Rachet B, Jooste V, Faivre J, Coleman MP. Continuing rapid increase in esophageal adenocarcinoma in England and Wales. Am J Gastroenterol 2008; 103: 2694-99.
4 – Engel LS, Chow WH, Vaughan TL, et al. Population at tributable risks of esophageal and gastric cancers. J Natl Cancer Inst 2003; 95: 1404-13.
5 – Whiteman DC, Sadeghi S, Pandeya N, et al, and the Australian Cancer Study. Combined effects of obesity, acid reflux and smoking on the risk of adenocarcinomas of the oesophagus. Gut 2008; 57: 173-80.
6 – Shaheen NJ, Richter JE. Barrett`s esophagus. Lancet 2009; 373: 850-61.
7 – Schnell TG, Sontag SJ, Chejfec G, et al. Long-term nonsurgical management of Barrett`s esophagus with high-grade dysplasia. Gastroenterology 2001; 120: 1607-19.
8 – Pennathur A, Farkas A, Krasinskas AM, et al. Esophagectomy for T1 esophageal cancer: outcomes in 100 patients and implications for endoscopic therapy. Ann Thorac Surg 2009; 87: 1048-55.
9 – Costa Jr Wl, Ribeiro HSC, Farias IC, Diniz AL, Godoy AL, Coimbra FJF. Adenocarcinoma de esôfago distal e transição esofagogástrica (TEG). In: Coimbra, FJF, ed. Câncer do aparelho digestivo alto. Rotinas do Departamento de Cirurgia Abdominal do A. C. Camargo Cancer Center. São Paulo: Atheneu, 2014: 15-27.
10 – Omloo JMT, Lagarde SM, Hulscher JB, et al. Extended transthoracic resection compared with limited transhiatal resection for adenocarcinoma of the mid/distal esophagus: five-year survival of a randomized clinical trial.Ann Surg 2007; 246: 992-1001.
11 – Pennathur A, Gibson MK, Jobe BA, Luketich JD. Oesophageal carcinoma. Lancet 2013; 381: 400-12.
12 – Kelsen DP, Winter KA, Gunderson LL, et al. Long-term results of RTOG trial 8911 (USA Intergroup 113): a random assignment trial comparison of chemotherapy followed by surgery compared with surgery alone for esophageal cancer. J Clin Oncol 2007; 25: 3719-25.
13 – Allum WH, Stenning SP, Bancewicz J, et al. Long-term results of a randomized trial of surgery with or without preoperative chemotherapy in esophageal cancer. J Clin Oncol 2009; 27: 5062-7.
14 – Cunningham D, Allum WH, Stenning SP, et al. Perioperative chemotherapy versus surgery alone for resectable gastroesophageal cancer. N Engl J Med 2006; 355: 11-20.
15 – Ychou M, Boige V, Pignon JP, et al. Perioperative chemotherapy compared with surgery alone for resectable gastroesophageal adenocarcinoma: an FNCLCC and FFCD multicenter phase III trial. J Clin Oncol 2011; 29: 1715-21.
16 – Burmeister BH, Smithers BM, Gebski V, et al. Surgery alone versus chemoradiotherapy followed by surgery for resectable cancer of the oesophagus: a randomised controlled phase III trial. Lancet Oncol 2005; 6: 659-68.
17 – Tepper J, Krasma MJ, Niedzwiecki D, et al. Phase III trial of trimodality therapy with cisplatin, fluorouracil, radiotherapy, and surgery compared with surgeryalone for esophageal cancer: CALGB 9781. J Clin Oncol 2008; 26: 1086-92.
18 – Van Hagen P, Hulshof MC, van Lanschot JJ, et al. Preoperative chemoradiotherapy for esophageal or junctional cancer. N Engl J Med 2012; 366: 2074-84.
19 – Stahl M, Walz MK, Stuschke M, et al. Phase III comparison of preoperative chemotherapy compared with chemoradiotherapy in patients with locally advanced adenocarcinoma of the esophago gastric junction. J Clin Oncol 2009; 27: 851-6.
20 – Burmeister BH, Thomas JM, Burmeister EA, et al. Is concurrent radiation therapy required in patients receiving preoperative chemotherapy for adenocarcinoma of the esophagus? A randomised phase II trial. Eur J Cancer 2011; 47: 354-60.
21 – Sjoquist KM, Burmeister BH, Smithers BM, et al. Survival after neoadjuvant chemotherapy or chemoradiotherapy for resectable oesophageal carcinoma: an updated meta-analysis. Lancet Oncol 2011; 12:681-92.
22 – Yamasaki M, Miyata H, Miyazaki Y, et al. Perioperative therapy for esophageal cancer. Gen Thorac Cardiovasc Surg 2014. DOI 20.1007/s11748-014-0458-y
23 – MacDonald JS, Smalley SR, Benedetti J, et al. Chemoradiotherapy after surgery compared with surgery alone for adenocarcinoma of the stomach or gastroesophageal junction. N Engl J Med 2001; 345: 725-30.
24 – Coimbra FJF, Diniz AL, Ribeiro HSC, Costa Jr WL, Godoy AL, Farias IC editores. Câncer do Aparelho Digestivo Alto. Manual de condutas terapêuticas do departamento de Cirurgia Abdominal do A.C. Camargo Cancer Center. São Paulo; Atheneu:2013
25 – Birkemeyer JD, Siewers AE, Finlayson EV, et al. Hospital volume and surgical mortality in the United States. N Eng J Med 2002;346(15): 1128-37.
26 –Reames BN, Ghaferi AA, Birkemeyer JD, et al. Hospital volume and operative mortality in the modern Era. Ann Surg 2014; 260(2): 244 – 251.
27 – Stein HJ, Feith M, Siewert JR. Cancer of esophago gastric junction. Surg Oncol 2000; 9(1):35-41.
28 – Hulscher JBF, van Sandick JW, de Boer AGEM, et al. Extended transthoracic resection compared with limited transhiatal resection for adenocarcinoma of esophagus. N Engl J Med 2002; 347:1662-9.
29 –Omloo JM, Lagarde SM, Hulscher JBF, et al. Extended transthoracic resection compared with limited transhiatal resection for adenocarcinoma of the mid/distal esophagus: five-year survival of a randomized clinical trial. Ann Surg 2007; 246(6): 992 – 1000.
30 – Yang C, Chen HN, Chen XZ, et al. Transtoracic resection versus non-transtoracic resection for gastroesophagel junction cancer: a meta-analysis. PloSone 2012;7(6):e37698
31 - Cuschieri A, Shimi S, Banting S. Endoscopic oesophagectomy through a right thoracoscopic approach.J R Coll Edinb. 1992;37:7–11.
32 - Biere SSAY, Henegowen MIB, Mass KW, et al. Minimally invasive versus open oesophagectomy for patients with oesophageal cancer: a multicentre, open-label, randomised controlled trial. Lancet 2012;379:1887-92.
33. Koyanagi K, Osawa S, Tachimori Y. Minimally invasive esophagectomy performed with the patient in a prone position: a systematic review. Surg Today 2015 Apr 10. (Epud ahead of print).
34. Kumar A, Asaf BB. Robotic Thoracic Surgery: the state of the art. J Minim Access Surg 2015; 11(1):60-67.
35. Al-Batran SE, Homann N, Pauligk C, et al. Perioperative chemotherapy with fluorouracil plus leucovorin, oxaliplatin, and docetaxel versus fluorouracil or capecitabine plus cisplatin and epirubicin for locally advanced, resectable gastric or gastro-oesophageal junction adenocarcinoma (FLOT4): a randomized, phase 2/3 trial. The Lancet Oncology 2019. (Epud ahead of print).
36. Noordman et al. Neoadjuvant chemoradiotherapy plus surgery versus active surveillance for oesophageal cancer: a stepped-wedge cluster randomized trial. BMC Cancer (2018) 18:142.
37. van der Sluis PC, et al. Robot-assited minimally invasive thoraco-laparoscopic esophageactomy versus open transthoracic esophagectomy for resectable esophageal cancer, a randomized controlled trial (ROBOT Trial). Trials 2012, 13:230.
38. Takesue T, et al. A prospective randomized trial of enteral nutrition after thoracoscopic esophagectomy for esophageal cancer. Ann Surg Oncol 2015; 23(suppl 5):1055








