 O CO-1686, um novo medicamento oral, inibidor de tirosina-quinase covalente, demonstrou boa tolerabilidade e eficácia promissora contra o câncer de pulmão não-pequenas células (CPNPC) com expressão EGFR-T790M positiva. O novo agente integra a chamada terceira geração dos inibidores de tirosina-quinase (TKI).
O CO-1686, um novo medicamento oral, inibidor de tirosina-quinase covalente, demonstrou boa tolerabilidade e eficácia promissora contra o câncer de pulmão não-pequenas células (CPNPC) com expressão EGFR-T790M positiva. O novo agente integra a chamada terceira geração dos inibidores de tirosina-quinase (TKI).
A eficácia dos inibidores de tirosina-quinase em CPNPC com mutação do EGFR é limitada pela emergência da mutação T790M em aproximadamente 60% dos pacientes. Além disso, erupção cutânea e diarreia são problemas comuns causados pela inibição do EGFR selvagem (wt). Para evitar esses efeitos adversos, o novo agente poupa seletivamente o EGFR selvagem (wt) e tem como alvo a ativação das mutações EGFR e T790M.
A primeira etapa do estudo para avaliar a ação do CO-1686 em pacientes com CPNPC avançado foi recentemente concluída e seus resultados apresentados durante a 4ª Conferência Europeia de Câncer de Pulmão. Os endpoints do estudo de fase I foram segurança, farmacocinética e eficácia.
 No total, 62 pacientes com mutação EGFR foram incluídos, com idade média de 59 anos. Os critérios de inclusão consideraram casos de CPNPC em estadio avançado, previamente tratados com um inibidor de quinase. As mulheres compreenderam 77% da população investigada e os pacientes asiáticos, 16%. O status de perfomance ECOG 0 foi registrado em 27% dos pacientes.
No total, 62 pacientes com mutação EGFR foram incluídos, com idade média de 59 anos. Os critérios de inclusão consideraram casos de CPNPC em estadio avançado, previamente tratados com um inibidor de quinase. As mulheres compreenderam 77% da população investigada e os pacientes asiáticos, 16%. O status de perfomance ECOG 0 foi registrado em 27% dos pacientes.
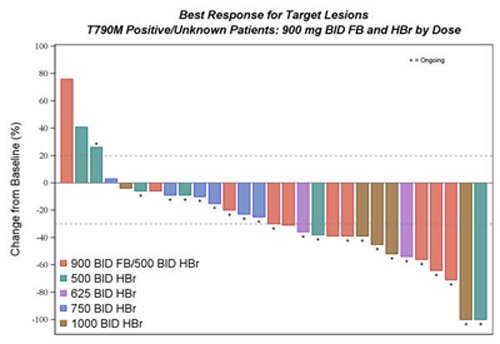
A genotipagem do EGFR foi realizada de forma centralizada, e o CO-1686 administrado oralmente, em ciclos sucessivos de 21 dias. As características dos pacientes na fase I indicam que aproximadamente 75% adquiriram resistência progressiva às terapias anteriores com TKIs e nesse subgrupo as taxas de resposta com o novo agente foram bastante promissoras. A eficácia foi clara nos pacientes com mutação T790M+, com taxa de resposta global de 64%. A taxa de resposta permanece acima de 50% mesmo quando pacientes com status T790M desconhecido foram incluídos.
Os resultados preliminares também demonstram que o CO-1686 é muito bem tolerado. A hiperglicemia grau 3 foi reportada por 19% dos pacientes. Outras toxicidades observadas foram náuseas, diarreia, falta de apetite, vômitos, fadiga e mialgia, todas leves na maioria dos casos. Os percentuais de diarreia e erupção cutânea indicam que não há inibição do EGFR selvagem. Apenas um paciente descontinuou a droga devido a eventos adversos.
Segundo a principal autora do estudo, Heather Wakelee, do Thoracic Oncology Unit, da Universidade de Stanford,
EUA, “o CO-1686 apresenta atividade promissora em todos os níveis de dose, com benefício duradouro”. A pesquisadora informou que ainda este ano o estudo com o CO-1686 deve recrutar pacientes para as fases II e III da investigação.
Referência: Abstract 93O:First-in-human evaluation of CO-1686, an irreversible, highly selective tyrosine kinase inhibitor of mutations of EGFR (activating and T790M). - http://oncologypro.esmo.org/Meeting-Resources/ELCC-2014/First-in-human-evaluation-of-CO-1686-an-irreversible-highly-selective-tyrosine-kinase-inhibitor-of-mutations-of-EGFR-activating-and-T790M








