Em edição especial que comemora 5 anos da coluna ‘Drops de Genômica’, o oncologista Andre Murad (foto) explica o que é o DNA tumoral circulante (ctDNA), suas aplicações clínicas, benefícios e direções futuras. Confira.
Por André Marcio Murad*
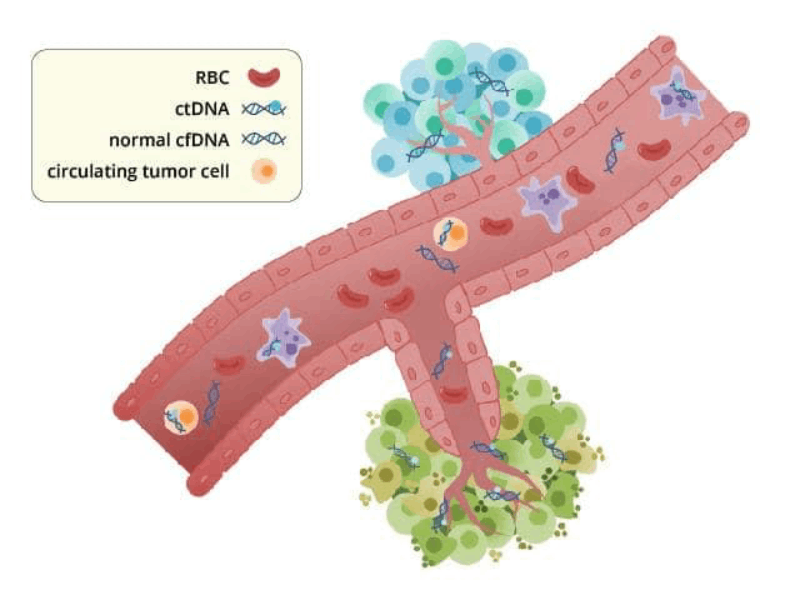
À medida que as células tumorais passam por seu ciclo de vida, fragmentos de DNA ganham a corrente sanguínea. Isso é conhecido como DNA tumoral circulante – ou ctDNA, para abreviar.
O teste de ctDNA, que usualmente é realizado através das técnicas de NGS ou PCR digital, examina o sangue de um paciente para detectar e sequenciar esses fragmentos de DNA das células tumorais. A tecnologia ainda é relativamente nova, mas as informações encontradas no sangue podem ajudar a orientar o tratamento do câncer. Através desse exame, podemos diagnosticar, monitorar ou potencialmente identificar novos alvos para terapia com base nos pequenos fragmentos de DNA que flutuam no próprio sangue.
O DNA tumoral circulante (ctDNA) é um biomarcador revolucionário e que transformou o cenário do diagnóstico e tratamento do câncer. O ctDNA fornece uma janela não invasiva para a análise da composição genética dos tumores. O ctDNA redimensionou, assim, o campo do diagnóstico e do tratamento do câncer, oferecendo um novo biomarcador de forma não invasiva, sensível e específico nas suas diversas aplicações, o que transforma o panorama geral do diagnóstico, prognóstico e tratamento do câncer, melhorando sobremaneira seus resultados e concorrendo para o incremento da sobrevida e qualidade de vida dos pacientes.
As aplicações clínicas do ctDNA:
1. Detecção e triagem precoce: o ctDNA pode ser usado para detecção precoce e triagem de vários tipos de câncer, incluindo câncer colorretal, de pulmão, de mama e de ovário. Ele pode detectar o câncer em um estágio inicial, mesmo antes do aparecimento dos sintomas, melhorando os resultados do tratamento e as taxas de sobrevivência.
2. Biópsia Líquida: a análise de ctDNA fornece uma biópsia líquida, reduzindo a necessidade de biópsias invasivas de tecido. Isto é especialmente benéfico para pacientes com tumores inacessíveis ou que necessitam de biópsias repetidas.
3. Monitoramento da resposta ao tratamento: o ctDNA pode monitorar a eficácia do tratamento e detectar resistência ou recorrência mais cedo do que os métodos de imagem tradicionais. Isto permite que os prestadores de cuidados de saúde ajustem prontamente as estratégias de tratamento.
4. Medicina personalizada e de precisão: a análise de ctDNA identifica mutações genéticas específicas, permitindo terapias direcionadas e abordagens de tratamento personalizadas. Este avanço propicia como consequência um tratamento mais eficaz e com efeitos colaterais potencialmente reduzidos.
5. Detecção de doença residual mínima (DRM): o ctDNA pode detectar DRM, ajudando a identificar pacientes com risco de recorrência. Isto permite que os prestadores de cuidados de saúde iniciem medidas terapêuticas de forma mais precoce ou ajustem os planos de tratamento.
Benefícios do ctDNA:
1. Não invasivo: a análise do ctDNA é um procedimento não invasivo, reduzindo o risco de complicações e melhorando o conforto, a comodidade e a redução de riscos por procedimentos invasivos para os pacientes.
2. Alta sensibilidade, especificidade e acurácia: a análise de ctDNA mostrou alta sensibilidade e especificidade, tanto na detecção de câncer quanto no monitoramento da resposta ao tratamento.
3. Monitoramento em tempo real: a análise de ctDNA fornece “insights” em tempo real sobre a dinâmica do tumor, inclusive com a detecção precoce de variantes genômica de resistência secundária, permitindo que os profissionais de saúde respondam mais prontamente a estas mudanças.
4. Custo-benefício: a análise de ctDNA pode reduzir os custos de saúde, minimizando a necessidade de repetidas biópsias e exames de imagem.
Direções futuras:
1. Detecção de múltiplos tipos de câncer: estão em andamento pesquisas para o desenvolvimento de testes de ctDNA que possam detectar vários tipos de câncer de forma mais precoce e simultaneamente - Multi-cancer early detection (MCED).
2. Combinação com outros biomarcadores: o ctDNA tem sido combinado a outros biomarcadores, como células tumorais circulantes e biomarcadores transcriptômicos (de RNA) e de proteínas, para aumentar a precisão do diagnóstico. Essa é a chamada análise multiômica, a qual pode inclusive ser utilizada pela tecnologia de célula única (single cell).
3. Integração com a Inteligência artificial (AI); a AI tem sido paulatinamente integrada à análise de ctDNA para uma melhor interpretação de seus resultados e de sua modelagem preditiva.