Em mais um tópico da coluna ‘Drops de Genômica’, o oncologista Andre Murad (foto) explica o splicing alternativo, processo celular no qual éxons do mesmo gene são unidos em diferentes combinações. Confira.
Por André Marcio Murad*
O chamado splicing (ou emenda) alternativo é um processo celular no qual éxons do mesmo gene são unidos em diferentes combinações, levando a transcrições de mRNA diferentes, mas relacionadas. Esses mRNAs podem ser traduzidos para produzir diferentes proteínas com estruturas e funções distintas - e tudo a partir de um único gene.
Suponhamos que um gene tenha sete éxons, que por sua vez codificam proteínas específicas. A partir destes sete éxons, podem ser criadas literalmente centenas de combinações de novas proteínas porque o splicing alternativo permite que diferentes éxons sejam ligados de diferentes maneiras. Este fenômeno faz com que o corpo humano tenha um conjunto muito mais complexo e diversificado de proteínas disponíveis, tanto para funções estruturais, como para funções imunitárias, ou apenas em geral sendo capaz de construir um sistema vivo que não é limitado por um certo número de proteínas.
A regulação anormal do splicing alternativo é geralmente acompanhada pela ocorrência e desenvolvimento de tumores, que produzem múltiplas isoformas diferentes e diversificam a expressão proteica. As alterações proteicas produzidas como consequência geram, então, múltiplas funções nas células tumorais, desde a proliferação e apoptose até a invasão e metástase, além da angiogênese e de seu metabolismo.
Os eventos de splicing anormais contribuem para a progressão do tumor como fatores oncogênicos e/ou fatores secundários. As alterações nos fatores de splicing detectados em tumores e outros eventos de splicing incorreto (isto é, RNAs não codificantes e circulares longos) na tumorigênese podem, por sua vez, abrir uma auspiciosa avenida para a descoberta de abordagens terapêuticas que promovam a catálise de splicing e o splicing de proteínas reguladoras para modular eventos de splicing patogênico (incluindo neoantígenos específicos de tumor para imunoterapia contra o câncer). As estratégias emergentes baseadas em RNA para o tratamento do câncer com isoformas de splicing anormalmente alternativos também têm sido recentemente exploradas. 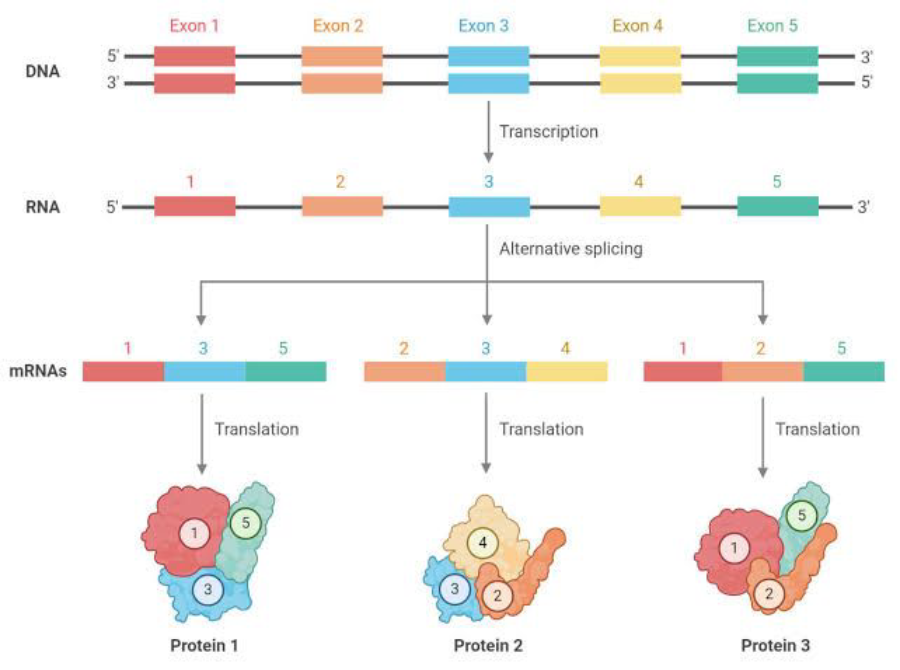
*André Murad é diretor científico do Grupo Brasileiro de Oncologia de Precisão (GBOP), diretor clínico da Personal - Oncologia de Precisão e Personalizada, professor adjunto coordenador da Disciplina de Oncologia da Faculdade de Medicina da UFMG, e oncologista e oncogeneticista da CETTRO Oncologia (DF)









