Marcelo Capra, do Centro Integrado de Hematologia e Oncologia do Hospital Mãe de Deus, em Porto Alegre, é primeiro autor de análise de subgrupos do estudo randomizado de Fase 3 (IKEMA) apresentada no congresso da Sociedade Americana de Hematologia (ASH 2022) que avaliou isatuximabe (Sarclisa®, Sanofi) mais carfilzomibe e dexametasona no tratamento do mieloma múltiplo recidivado, de acordo com as linhas prévias de tratamento. Os resultados desta análise de subgrupo são consistentes com o benefício observado na população geral do estudo IKEMA e apoiam ainda mais Isa-Kd como um tratamento padrão para pacientes com MM recidivado e/ou refratário.
Marcelo Capra, do Centro Integrado de Hematologia e Oncologia do Hospital Mãe de Deus, em Porto Alegre, é primeiro autor de análise de subgrupos do estudo randomizado de Fase 3 (IKEMA) apresentada no congresso da Sociedade Americana de Hematologia (ASH 2022) que avaliou isatuximabe (Sarclisa®, Sanofi) mais carfilzomibe e dexametasona no tratamento do mieloma múltiplo recidivado, de acordo com as linhas prévias de tratamento. Os resultados desta análise de subgrupo são consistentes com o benefício observado na população geral do estudo IKEMA e apoiam ainda mais Isa-Kd como um tratamento padrão para pacientes com MM recidivado e/ou refratário.
No ensaio clínico randomizado de Fase III IKEMA, com participação de 69 centros em 16 países, foram elegíveis 302 pacientes adultos (≥18 anos) com mieloma múltiplo recidivado ou refratário, com proteína M sérica ou urinária mensurável, previamente expostos a até 3 linhas de tratamento. Os pacientes foram randomizados (3:2) para receber isatuximabe mais carfilzomibe-dexametasona (grupo Isa-Kd; N= 179) ou carfilzomibe-dexametasona (grupo Kd; N=123). Os pacientes do grupo Isa-Kd receberam isatuximabe 10 mg/kg por via intravenosa semanalmente nas primeiras 4 semanas, depois a cada 2 semanas por ciclos de 28 dias em combinação com carfilzomibe duas vezes por semana na dose de 20/56mg/m2 e dexametasona na dose padrão para a duração do tratamento. O tratamento continuou até progressão ou toxicidade inaceitável. O endpoint primário foi sobrevida livre de progressão (SLP) avaliada na população com intenção de tratar. Endpoints secundários incluíram taxa de resposta global, taxa de resposta completa e parcial, taxa de negatividade de doença residual mínima e sobrevida global, além da análise de segurança.
Os dois grupos foram bem equilibrados em termos de idade (mediana de 65 anos no braço Isa-Kd e de 63 anos no braço Kd), assim como foram bem equilibrados considerando função renal, estadiamento ISS e perfil citogenético.
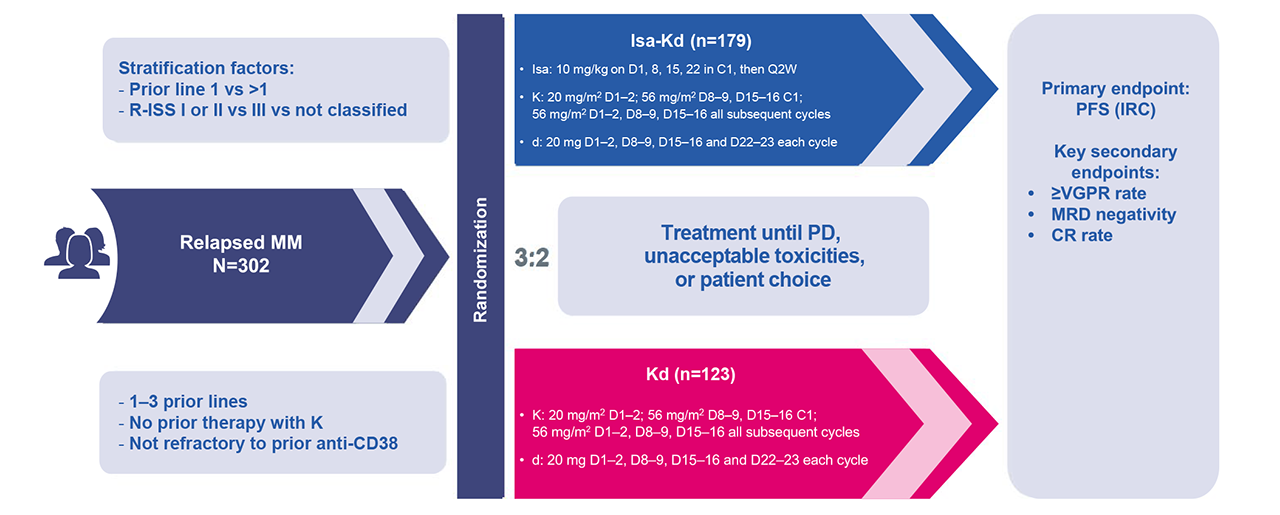
A análise final de sobrevida livre de progressão (SLP) do estudo de Fase 3 IKEMA (NCT03275285), realizada 2 anos após a análise interina pré-planejada, confirmou que isatuximabe (Isa) + carfilzomibe (K) e dexametasona (d) (Isa-Kd) melhorou significativamente a SLP em comparação com Kd em pacientes com MM recidivado (razão de risco [HR] 0,58; intervalo de confiança [IC] de 95,4%, 0,42–0,79), com aumento clinicamente significativo na negatividade mínima da doença residual (MRD–) (33,5% vs 15,4 %) e na taxa de resposta completa (CR) (44,1% vs 28,5%) na população com intenção de tratar, com perfil de segurança manejável1. Os resultados embasaram a aprovação de isatuximabe pela Anvisa (DOU nº129)2 e outras autoridades regulatórias de diversos países.
Na análise selecionada para o ASH 20223 foram apresentados os resultados atualizados de eficácia e segurança do IKEMA por número de linhas anteriores de tratamento (1 vs >1). Foram considerados pacientes com 1 a 3 linhas anteriores de tratamento, randomizados 3:2 para receber Isa-Kd (n=179) ou Kd (n=123). O tratamento foi administrado até progressão da doença ou toxicidade inaceitável. Os dados atualizados e de longo prazo são baseados na análise de SLP pré-especificada (endpoint primário) de IKEMA, com 159 eventos.
Resultados
Dos 302 pacientes randomizados, 134 (44,4%; 79 Isa-Kd, 55 Kd) receberam 1 linha de tratamento anterior e 168 (55,6%; 100 Isa-Kd, 68 Kd) receberam > 1 linha de tratamento anterior. Em um acompanhamento médio de 44 meses em cada subgrupo (data limite de 14 de janeiro de 2022), os autores descrevem que a SLP melhorou com Isa-Kd vs Kd em ambos os subgrupos, consistente com o endpoint primário na população com intenção de tratar. Entre os pacientes que receberam 1 linha de tratamento anterior, a mediana de SLP foi de 38,24 meses com Isa-Kd e 28,19 meses com Kd (HR não estratificado 0,723; 95,4% CI 0,442–1,184; P= 0,0983). Em pacientes que receberam >1 linha anterior de terapia, a SLP mediana foi de 29,21 meses com Isa-Kd e 16,99 meses com Kd (HR não estratificado 0,452; IC 95,4% 0,298–0,686; P< 0,0001).
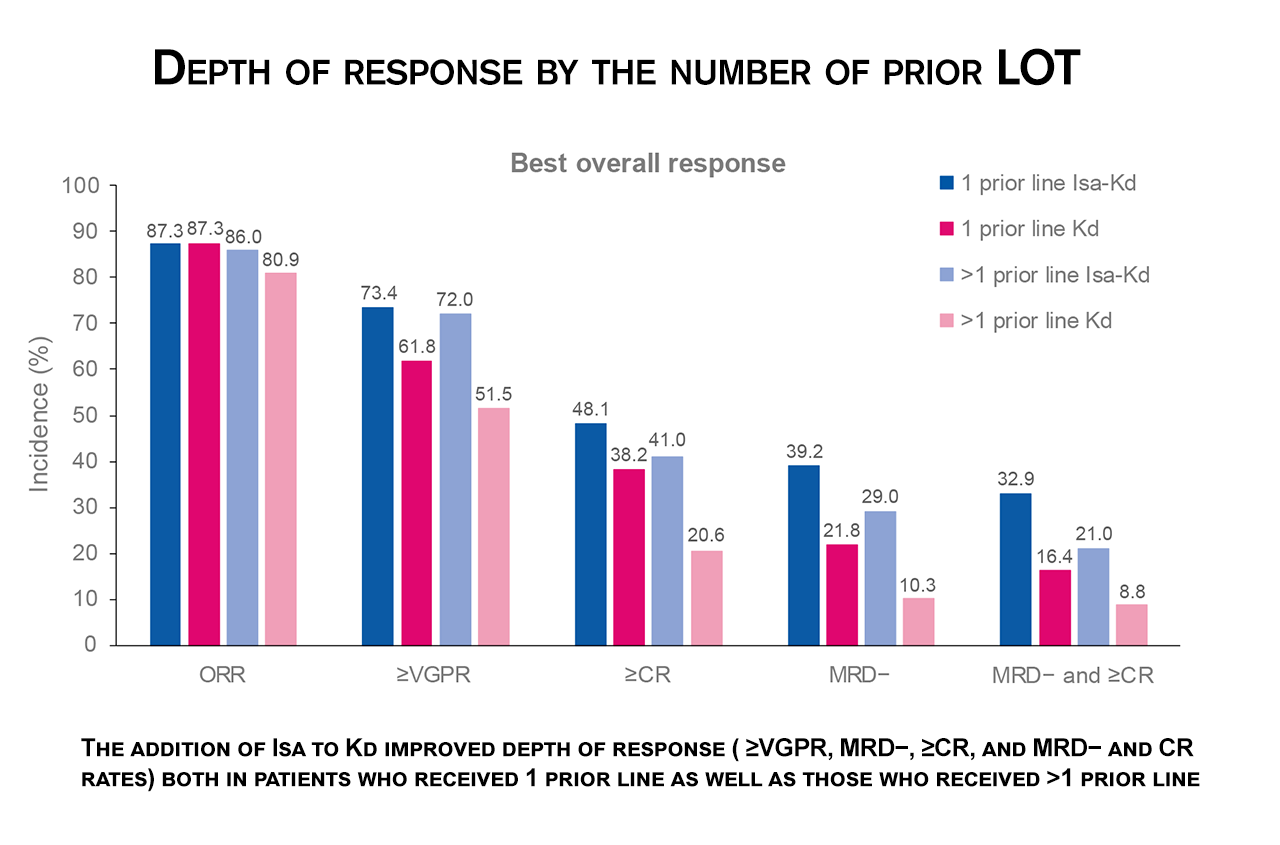
A profundidade da resposta melhorou com a adição de Isa a Kd em ambos os subgrupos. Capra et al. destacam que mais pacientes alcançaram CR com Isa-Kd do que com Kd (48,1% vs 38,2%, 1 linha anterior; 41,0% vs 20,6%, >1 linha anterior). A adição de Isa a Kd também rendeu taxas mais altas de MRD– (39,2% vs 21,8%, 1 linha anterior; 29,0% vs 10,3%, >1 linha anterior) e MRD– e CR (32,9% vs 16,4%, 1 linha anterior linha; 21,0% vs 8,8%, >1 linha anterior).
Em relação à segurança, quase todos os pacientes apresentaram pelo menos um evento adverso emergente do tratamento (TEAE). A frequência de TEAEs de grau ≥3 foi semelhante entre os subgrupos (83,3% [Isa-Kd] e 72,2% [Kd], 1 linha anterior; 83,8% [Isa-Kd] e 73,5% [Kd], > 1 linha anterior). TEAEs graves ocorreram em 66,7% vs 51,9% dos pacientes (subgrupo de 1 linha prévia) e 72,7% vs 66,2% dos pacientes (>1 linha anterior) com Isa-Kd vs Kd, respectivamente. A porcentagem de pacientes com TEAEs que levaram à descontinuação do tratamento foi numericamente menor com Isa-Kd do que com Kd: 9,0% vs 13,0% (1 linha anterior) e 15,2% vs 22,1% (>1 linha anterior).
No subgrupo que recebeu 1 linha de tratamento anterior, 4 pacientes (5,1%) no braço Isa-Kd tiveram um TEAE com desfecho fatal. No subgrupo >1 linha de tratamento anterior, 6 pacientes (6,1%) no braço Isa-Kd e 6 pacientes (8,8%) no braço Kd tiveram TEAE com desfecho fatal durante o período de tratamento.
“Separando por linhas prévias de tratamento, demonstramos que o perfil de tolerabilidade foi manejável tanto em pacientes que receberam apenas uma linha de tratamento prévio, como em pacientes com mais de uma linha prévia de tratamento, indicando que o esquema é bem tolerado mesmo em uma população mais exposta a drogas e, potencialmente, com mais complicações da doença”, observou Capra.
Em síntese, a adição de isatuximabe a carfilzomibe e dexametasona melhorou a sobrevida livre de progressão e a profundidade de resposta nos pacientes com mieloma múltiplo recidivado e refratário, com um perfil de toxicidade aceitável independentemente do número de linhas prévias de tratamento, incluindo a primeira recidiva. “São dados significativos e consistentes com a análise primária do estudo que suportam o uso de isatuximabe, carfilzomibe e dexametasona como um tratamento muito importante nos pacientes com mieloma recidivado e refratário”, conclui Capra.
ASSISTA SOBRE O MESMO TEMA
ASH 2022: análise de subgrupo do estudo IKEMA por linhas prévias de tratamento
Em vídeo, o hematologista Marcelo Capra comenta análise de subgrupos do estudo randomizado de Fase 3 IKEMA selecionada para apresentação em pôster no ASH 2022 que avalia isatuximabe (Sarclisa®, Sanofi) mais carfilzomibe e dexametasona no tratamento do mieloma múltiplo recidivado, de acordo com as linhas prévias de tratamento. Assista, na TV ONCONEWS.
Referências:
1 - Moreau, P., Dimopoulos, M.-A., Mikhael, J., Yong, K., Capra, M., Facon, T., … Kim, K. (2021). Isatuximab, carfilzomib, and dexamethasone in relapsed multiple myeloma (IKEMA): a multicentre, open-label, randomised phase 3 trial. The Lancet, 397(10292), 2361–2371. doi:10.1016/s0140-6736(21)00592-4
2 - DIÁRIO OFICIAL DA UNIÃO - Publicado em: 11/07/2022 | Edição: 129 | Seção: 1 | Página: 80
3 - 3176 Isatuximab Plus Carfilzomib and Dexamethasone in Relapsed Multiple Myeloma: Ikema Subgroup Analysis By Number of Prior Lines of Treatment
Program: Poster Abstracts
Session: 652. Multiple Myeloma and Plasma Cell Dyscrasias: Clinical and Epidemiological: Poster II
Sunday, December 11, 2022, 6:00 PM-8:00 PM
Marcelo Capra, MD, PhD et al
--








