Depois de receber aprovação das principais agências reguladoras do mundo1,2 e também da brasileira Anvisa3, ixazomibe (Ninlaro®) passa a integrar a lista de cobertura obrigatória da Agência Nacional de Saúde (ANS), em decisão que incorpora o primeiro inibidor de proteassoma de uso oral ao tratamento de pacientes com mieloma múltiplo recidivado ou refratário (MMRR) 4 atendidos na saúde suplementar. A adição de ixazomibe a um regime de lenalidomida e dexametasona foi associada a sobrevida livre de progressão significativamente mais longa em pacientes com MMRR, além de resultados históricos de sobrevida global, como sustentam evidências do ensaio TOURMALINE-MM1 (ClinicalTrials.gov: NCT01564537)5.
Depois de receber aprovação das principais agências reguladoras do mundo1,2 e também da brasileira Anvisa3, ixazomibe (Ninlaro®) passa a integrar a lista de cobertura obrigatória da Agência Nacional de Saúde (ANS), em decisão que incorpora o primeiro inibidor de proteassoma de uso oral ao tratamento de pacientes com mieloma múltiplo recidivado ou refratário (MMRR) 4 atendidos na saúde suplementar. A adição de ixazomibe a um regime de lenalidomida e dexametasona foi associada a sobrevida livre de progressão significativamente mais longa em pacientes com MMRR, além de resultados históricos de sobrevida global, como sustentam evidências do ensaio TOURMALINE-MM1 (ClinicalTrials.gov: NCT01564537)5.
Neste estudo de Fase III duplo-cego, controlado por placebo, foram incluídos 722 pacientes com MMRR, estratificados pelo número de terapias anteriores (1 versus 2 ou 3), exposição prévia a inibidor de proteassoma (sim vs não) e estágio da doença I ou II vs III, segundo critérios do Sistema Internacional de Estadiamento (Fig 1). Os pacientes elegíveis foram randomizados (1:1) para receber ixazomibe mais lenalidomida-dexametasona (grupo ixazomibe, N= 360) ou placebo mais lenalidomida-dexametasona (grupo placebo-controle, N= 362). O endpoint primário foi a sobrevida livre de progressão. Endpoints secundários incluíram sobrevida global (SG) e sobrevida global em pacientes com citogenética de alto risco e de alto risco expandido, além de análises de segurança e dados de qualidade de vida relatados pelo paciente, a partir de questionário validado (Q30 da EORTC).
Fig1.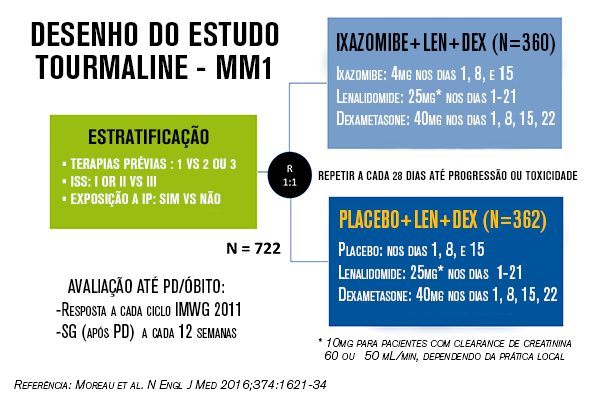
A resposta foi avaliada a cada ciclo até a progressão da doença, de acordo com os critérios do International Myeloma Working Group 20116.
Na primeira análise, os resultados de sobrevida livre de progressão cruzaram o limite pré-especificado e em um seguimento mediano de 14,8 meses mostraram que o regime de ixazomibe foi associado a um benefício significativo na comparação com o grupo placebo-controle. A mediana de SLP foi de 20,6 meses vs 14,7 meses (HR: 0,74, IC 95%, 0,59 a 0,94; P = 0,01), representando SLP 40% maior no grupo tratado com ixazomibe mais lenalidomida-dexametasona (FIG 2). Os dados de SLP, principal endpoint de eficácia, foram reportados em abril de 2016 na New England Journal of Medicine (NEJM), em artigo de Philippe Moreau e colegas do TOURMALINE-MM1 Study Group7.
Fig2.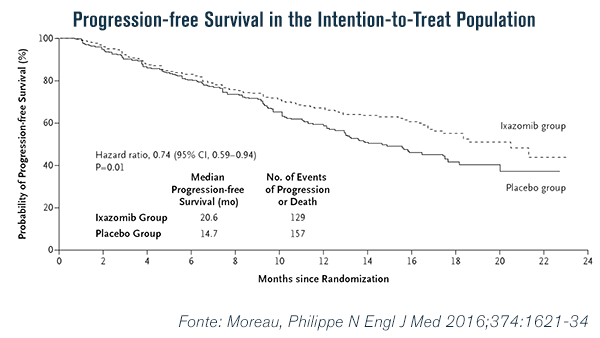
Análises de subgrupos confirmaram o benefício de SLP mesmo em pacientes com perfil citogenético de alto risco. A mediana de SLP nesse subgrupo (75 pacientes no grupo ixazomibe e 62 pacientes no grupo placebo) foi de 21,4 meses e 9,7 meses, respectivamente (HR 0,54; IC de 95%, 0,32 a 0,92; P = 0,02); entre os pacientes com del (17p) (36 no grupo ixazomibe e 33 no grupo placebo) a mediana de SLP foi de 21,4 meses e 9,7 meses, respectivamente (HR 0,60; IC 95%, 0,29 a 1,24), e entre os pacientes com t (4; 14) sem del (17p) ou t (14; 16) (36 no grupo ixazomibe e 25 no grupo placebo) a SLP mediana foi de 18,5 meses e 12,0 meses, respectivamente (HR 0,65; IC 95%, 0,25 a 1,66).
As taxas de resposta global também favoreceram o grupo tratado com ixazomibe frente ao grupo controle (78% vs 72%), com 48% de resposta completa e 39% de resposta parcial no braço de intervenção. O tempo médio de resposta foi de 1,1 meses no grupo ixazomibe e de 1,9 meses no grupo placebo, com duração mediana de 20,5 meses e 15,0 meses respectivamente, evidenciando respostas rápidas e sustentadas com ixazomibe.
Esses resultados subsidiaram a decisão da Diretoria Colegiada da Agência Nacional de Saúde Suplementar (ANS), que em fevereiro de 2021 aprovou ixazomibe (Ninlaro®) no tratamento do mieloma múltiplo como parte do novo rol de cobertura obrigatória dos planos de saúde. Com a nova Resolução Normativa (RN nº 465/2021) e a atualização do Rol de Procedimentos e Eventos em Saúde, ixazomibe passa a integrar a lista obrigatória dos planos de saúde no tratamento do mieloma múltiplo. A decisão da ANS está em vigor desde 1º de abril de 2021.
A dose inicial recomendada de ixazomibe é uma cápsula de 4mg administrada por via oral nos dias 1, 8 e 15 (veja tabela) de um ciclo de tratamento de 28 dias.8

Em artigo na Journal of Clinical Oncology (JCO)9, Paul G. Richardson e colegas reportaram em junho de 2021 outro importante endpoint de eficácia do ensaio TOURMALINE-MM1: a sobrevida global. Em um acompanhamento mediano de 85 meses, a SG no braço tratado com ixazomibe + lenalidomida foi de 53,6 versus 51,6 meses no braço placebo (HR, 0,939; P = 0,495). Os autores descrevem que a maior magnitude do benefício de SG com ixazomibe foi observada em subgrupos específicos: pacientes refratários a qualquer linha de tratamento (HR 0,794) ou a última linha de tratamento (0,742); idade> 65-75 anos (0,757); estágio III do Sistema Internacional de Estadiamento (0,779); 2 a 3 terapias anteriores (0,845); citogenética de alto risco (0,870); e citogenética de alto risco e / ou amplificação 1q21 (0,862).
“Esta análise final do estudo TOURMALINE-MM1, após acompanhamento médio maior que 7 anos, relata os dados medianos de SG mais longos vistos até hoje em estudos de Fase III avaliando combinações com lenalidomida em pacientes com mieloma múltiplo recidivado ou refratário, com mediana próxima a 4,5 anos em ambos os braços. Embora a discreta tendência de SG (HR 0,939) em favor de ixazomibe-lenalidomida na população ITT não tenha sido estatisticamente significativa, a maior magnitude do benefício de SG foi observada em subgrupos com características de alto risco, incluindo pacientes intensamente pré-tratados, aqueles refratários ao tratamento anterior, pacientes com MM em estágio III e aqueles com citogenética de alto risco ou de alto risco expandido”, destaca a publicação na NEJM.
A oncohematologista Flávia Xavier, professora adjunta de Hematologia da Universidade de Brasília (UNB), chefe do serviço de Hematologia e Hemoterapia do Hospital Universitário e médica da Rede D’Or em Brasília, destaca o impacto de ixazomibe. “Um dado muito importante é em relação à sobrevida livre de progressão, principalmente no grupo de alto risco, onde o aumento de SLP foi ainda mais significativo”, explica a especialista. “Este é o follow up mais longo já publicado e mostrou que quase 31% dos pacientes com MMRR continuavam vivos após uma mediana de 7 anos de tratamento com ixazomibe”, acrescenta. “Vale ressaltar que esse é um regime totalmente oral, o que traz a possibilidade de mais qualidade de vida ao evitar o deslocamento para os centros de infusão para realizar o tratamento. É um benefício que precisa ser considerado pelo ganho de sobrevida e na pandemia tem a vantagem adicional, pela facilidade de uso”, avalia.
Após o tratamento com a adição de ixazomibe, 71,7% versus 69,9% dos pacientes receberam ≥ 1 terapia anticâncer, principalmente daratumumabe e inibidor de proteassoma, o que concorreu para dificultar a análise final de sobrevida global. Fica a reflexão de que a disponibilidade de múltiplas terapias de resgate pode limitar a capacidade de demonstrar o benefício de SG no cenário de recaída precoce.
Em relação ao perfil de toxicidade, novas neoplasias primárias foram semelhantes com a adição de ixazomibe (10,3%) e placebo (11,9%) no momento da análise de sobrevida global e não foram reportados novos sinais de segurança. Trombocitopenia (21,3% vs 10,3%) e diarreia (10,0% vs 3,1%) foram os únicos eventos adversos de grau ≥ 3 relacionados ao tratamento, com ocorrência em ≥ 5% da população avaliada.
Mieloma múltiplo é uma malignidade hematológica que afeta os plasmócitos (células produtoras de anticorpos) da medula óssea. Globalmente, quase 230 mil pessoas convivem com a doença (Globocan, 2012) e cerca de 114 mil novos casos são diagnosticados a cada ano.10
Na fase inicial, nenhum sintoma pode ser observado, mas com a progressão o MM pode ocasionar dores nos ossos, anemia, disfunção renal e infecções. De causa desconhecida, o MM é mais frequente em indivíduos na faixa dos 60 anos de idade, mais comum em homens do que mulheres.
“O mieloma múltiplo é superimportante no nosso cenário da hematologia”, analisa Breno Gusmão, oncohematologista da BP – a Beneficência Portuguesa de São Paulo. “No nosso dia a dia, o MM é um dos carros-chefes da oncohematologia e das unidades de transplante. Com a entrada das novas drogas orais no rol da ANS, o tratamento do mieloma múltiplo é assunto cada vez mais relevante, tanto no cenário de primeira linha quanto no contexto da refratariedade e da recidiva”, destaca Gusmão.
Assista também sobre o mesmo assunto a um vídeo exclusivo:
TOURMALINE-MM1: resultados históricos no tratamento do mieloma múltiplo
A Agência Nacional de Saúde (ANS) incorporou o uso do inibidor de proteassoma de uso oral ixazomibe em associação lenalidomida e dexametasona para o tratamento de pacientes com mieloma múltiplo recidivado ou refratário (MMRR) atendidos na saúde suplementar. A decisão foi embasada nos resultados do estudo de Fase III TOURMALINE-MM1, tema de vídeo com os hematologistas Flávia Xavier e Breno Gusmão. Assista, na TV ONCONEWS.
Referências
1 - https://www.drugs.com/newdrugs/fda-approves-ninlaro-ixazomib-multiple-myeloma-4301.html
2 - https://www.ema.europa.eu/en/medicines/human/EPAR/ninlaro
3 - https://consultas.anvisa.gov.br/#/medicamentos/25351038663201613/
4 - https://www.gov.br/ans/pt-br/assuntos/noticias/beneficiario/planos-de-saude-novas-coberturas-entram-em-vigor
5 - https://www.clinicaltrials.gov/ct2/show/NCT01564537
6 - Rajkumar SV, Harousseau JL, Durie B, et al: Consensus recommendations for the uniform reporting of clinical trials: Report of the International Myeloma Workshop Consensus Panel 1. Blood 117:4691-4695, 2011
7 - Moreau, P., Masszi, T., Grzasko, N., Bahlis, N. J., Hansson, M., Pour, L., … Richardson, P. G. (2016). Oral Ixazomib, Lenalidomide, and Dexamethasone for Multiple Myeloma. New England Journal of Medicine, 374(17), 1621–1634. doi:10.1056/nejmoa1516282
8 - Ninlaro® citrato de ixazomibe – Bula para profissional da saúde https://www.takeda.com/4ab3a7/siteassets/pt-br/home/what-we-do/produtos/ni_caps_1219_0120_vps.pdf
9 - Paul G. Richardson et al. (2021). Final Overall Survival Analysis of the TOURMALINE-MM1 Phase III Trial of Ixazomib, Lenalidomide, and Dexamethasone in Patients With Relapsed or Refractory Multiple Myeloma. Journal of Clinical Oncology, DOI: 10.1200/JCO.21.00972
10 - Ferlay J, Soerjomataram I, Dikshit R, Eser S, Mathers C, Rebelo M, Parkin DM, Forman D, Bray F. Cancer incidence and mortality worldwide: sources, methods and major patterns in GLOBOCAN 2012. Int J Cancer. 2015 Mar 1;136(5):E359-86. doi: 10.1002/ijc.29210. Epub 2014 Oct 9. PMID: 25220842.








